Експеримент RT-qPCR включає екстракцію РНК та оцінку якості, зворотну транскрипцію та qPCR у три етапи, кожен крок має багато запобіжних заходів, які ми детально представимо нижче.
Ⅰ.Оцінка якості РНК
В експерименті RT-qPCR після завершення екстракції РНК необхідно оцінити якість РНК, а подальший експеримент можна проводити лише після його кваліфікації.Методи оцінки включають спектрофотометр, електрофорез у гелі Agilent, аналіз Agilent 2100, серед яких найчастіше використовують спектрофотометр та метод виявлення електрофорез у агарозному гелі.Слід зазначити, що ці два методи потрібно використовувати разом для завершення виявлення та аналізу концентрації, чистоти та цілісності РНК, щоб забезпечити якість РНК.
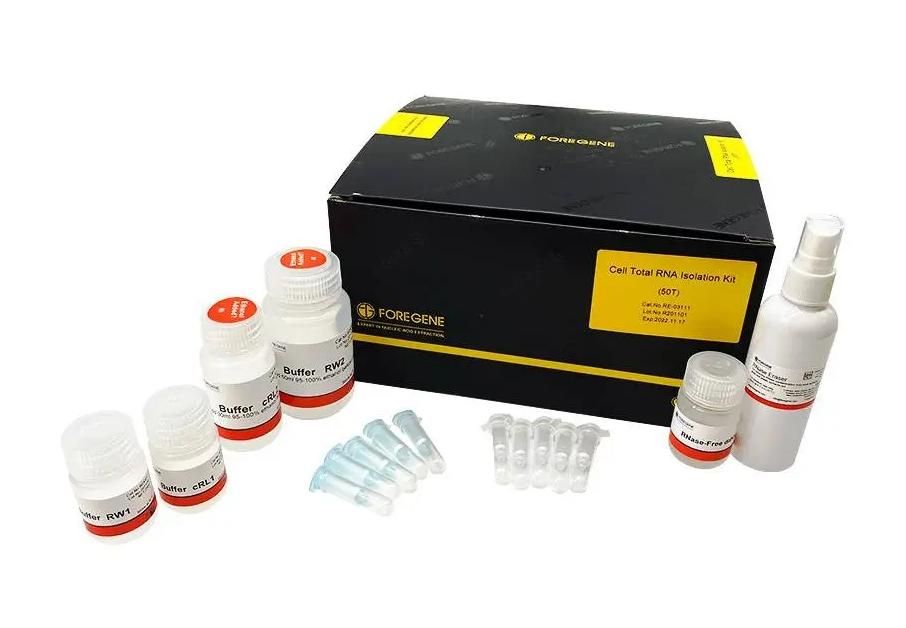
Пов'язаний набір для виділення РНК:
Набір для виділення тотальної РНК клітини
Високоочищену та високоякісну сумарну РНК можна отримати з різних культивованих клітин за 11 хв.
Набір для виділення тотальної РНК тварин
Швидко та ефективно витягуйте загальну РНК високої чистоти та високої якості з різних тканин тварин.
Спектрофотометр:
Спектрофотометр в основному використовується для визначення концентрації та чистоти РНК, але він не може виявити цілісність РНК і геномний залишок.Серед них A260/280 і A260/230 є важливими параметрами для виявлення чистоти РНК, і чистоту РНК можна визначити відповідно до коливання їх значень:
1. 1,9 < A260/280 < 2,1, що вказує на те, що чистота РНК хороша;A260/280<1,9, що вказує на те, що в РНК може бути білковий залишок;A260/280>2.1, що вказує на можливу часткову деградацію РНК, що може бути додатково підтверджено електрофорезом у агарозному гелі.
2. 2,0 < A260/230 < 2,2, що вказує на хорошу чистоту РНК;A260/230< 2,0, що вказує на те, що в РНК можуть бути залишки органічних реагентів, таких як феноли, етанол або цукри.
Електрофорез у агарозному гелі:
Аналіз електрофорезу в агарозному гелі може аналізувати цілісність РНК, геном і білкові залишки, але не може точно визначити концентрацію РНК або виявити залишки органічних реагентів.Візьмемо, наприклад, шаблони еукаріотичної РНК:
1. РНК піддали електрофорезу в агарозному гелі.Якщо на гелевій карті було лише три окремі смуги 28sRNA, 18sRNA та 5,8sRNA, це означає, що екстрагована РНК є інтактною.Якщо спостерігається феномен затягування, це свідчить про часткову деградацію РНК.
2. Якщо між отвором клею та смугою 28sRNA є одна яскрава смуга, можливо, там є залишок геномної ДНК.
3. Якщо в отворі клею з'явилися смуги, це свідчить про наявність залишків білка та інших високомолекулярних речовин.
Ⅱ. Зворотна транскрипція
Після завершення екстракції РНК її потрібно перетворити на кДНК для наступних експериментів, тому етап реверсії є важливим.Зворотна транскрипція буде введена з вибору зворотної транскриптази та праймера:
Вибір зворотної транскриптази:
Типові зворотні транскриптази включають AMV RTase і MMLV RTase.РНКаза H AMV RTase має сильну активність, коротку тривалість синтезу, низьку кількість синтезу та хорошу термостабільність (42 ~ 55 ℃).Активність РНКази Н RTase MMLV слабка, тривалість синтезу велика, кількість синтезу висока, а термостабільність низька (37 ~ 42 ℃).
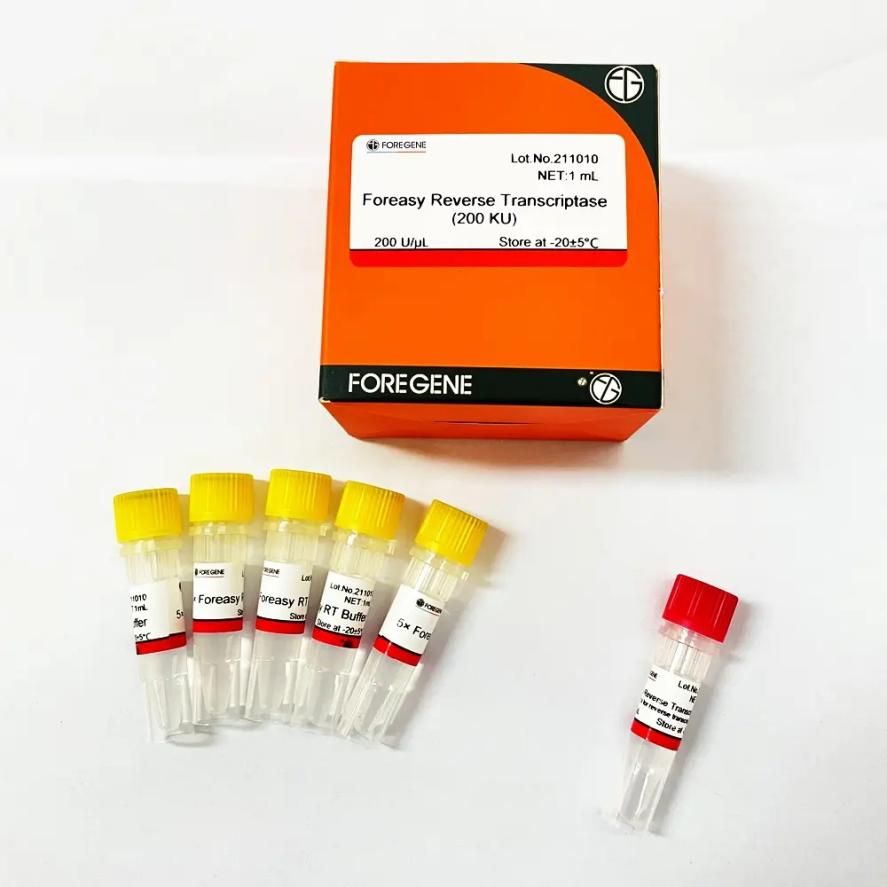
Оскільки фермент РНКаза H має функцію деградації матриці РНК, MMLV зі слабкою активністю РНКази H слід переважно відбирати під час зворотної транскрипції, а після подальшої генної інженерії термостабільність MMLV досягла якісного стрибка.Беручи ForegeneForeasy Reverse Transcriptase (M-MLV для зворотної транскрипції) наприклад, це нова зворотна транскриптаза, що експресується в бактеріях E. coli, сконструйованих за допомогою технології генетичної рекомбінації.Це рекомбінантна ДНК-полімераза, яка синтезує комплементарний ланцюг ДНК з одноланцюгової РНК, ДНК або гібриду РНК:ДНК.Він не має активності РНКази H, має високу стабільність, сильну спорідненість до РНК і високу чутливість виявлення.
Foreasy Reverse Transcriptase (M-MLV для зворотної транскрипції)
Вибір грунтовки:
Зазвичай RT-праймери поділяються на три категорії: оліго dT, випадкові праймери та ген-специфічні праймери.Виберіть відповідні праймери для використання відповідно до різних експериментальних вимог.
1. Якщо матриця еукаріотичного походження і пізня кДНК використовується для рутинної ПЛР-ампліфікації, рекомендується Oligo (dT);Якщо наступний експеримент використовується лише для кПЦР, Oligo (dT) рекомендується змішувати з довільними праймерами, щоб покращити ефективність зворотної транскрипції.
2. Якщо шаблон походить від прокаріотів, для зворотної транскрипції слід вибрати випадкові праймери або геноспецифічні праймери.
Ⅲ.КПЦР
Кількісне визначення флуоресценції в основному розроблено на основі вибору кількісних методів, принципів розробки праймерів, вибору ROX, конфігурації реакційної системи та налаштування умов реакції тощо.
Вибір кількісних методів:
Кількісні методи поділяються на відносні кількісні методи та абсолютні кількісні методи.Відносну кількісну оцінку можна використовувати для визначення впливу певних методів лікування на експресію генів, виявлення різниці експресії генів у різний час і порівняння різниці експресії генів у різних тканинах.Абсолютна кількісна оцінка може виявити кількість нуклеїнової кислоти у вірусі тощо.Проводячи експерименти, ми повинні вибрати відповідні кількісні методи відповідно до наших власних експериментів.
Принципи дизайну грунтовки:
Конструкція праймера для КПЦР безпосередньо пов’язана з ефективністю ампліфікації та специфічністю продукту.Тому правильний дизайн хороших праймерів є першим кроком успішної ПЛР.При розробці грунтовки слід звернути увагу на наступні принципи, дотримуючись принципу звичайної конструкції грунтовки:
1. Довжина цільового фрагмента контролюється між 100 і 300 bp;
2. Перехресний екзонний дизайн для уникнення впливу геномної ДНК;
3. Розроблені праймери необхідно перевірити на ефективність ампліфікації, і тільки коли ефективність ампліфікації досягне стандарту (90-110%), їх можна використовувати для кількісних експериментів;
4. Концентрація праймера зазвичай оптимізована між 0,1 мкМ і 1,0 мкМ.
ВибірROX:
У процесі кількісної реакції ROX може рівномірно регулювати різницю оптичного шляху, помилку піпетування або різницю об’єму, викликану випаровуванням і конденсацією, покращуючи повторюваність результатів.Однак слід зазначити, що вибір ROX пов'язаний з інструментом.Якщо прилад qPCR має функцію автоматичної корекції різниці між отворами, йому не потрібно додавати ROX;інакше потрібно додати корекцію ROX.Невеликі партнери в купівлі реагентів повинні бути відповідно до інструменту, який використовується, щоб вибрати правильний ROX, щоб уникнути подальших помилок.
Підготовка реакційної системи:
Переважними є реакційні об’єми 20 і 50 мкл.При створенні системи слід звернути увагу на такі моменти:
1. Реакційну систему потрібно підготувати за допомогою вентиляції в ультрачистому верстаку, новий ddH2O використовується для кожного експерименту;
2. Для кожного експерименту необхідно підготувати NTC, щоб перевірити, чи є в системі забруднення, і кожна пара праймерів повинна зробити NTC під час підготовки системи;
3. Щоб виявити, чи є залишок гДНК у матриці РНК, NRT можна підготувати для кожного зразка для виявлення;
4. При підготовці системи рекомендується зробити не менше 3 технічних повторів для одного зразка;
5. Якщо матрицею є кДНК, її рекомендується розбавити в 5-10 разів, щоб зменшити ефект інгібування системи зворотної транскрипції в експерименті з КПЦР.Краще досліджувати кількість шаблону за градієнтом, щоб значення CT було між 20-30;
6. Визначити необхідну кількість реакцій, збільшити на 5-10% на основі кількості реакцій і розрахувати кількість конфігурації об'єму;
7, система готується за принципом попереднього змішування, змішування після центрифугування та забезпечення відсутності бульбашок;
8. Наскільки це можливо, виберіть допоміжні витратні матеріали.
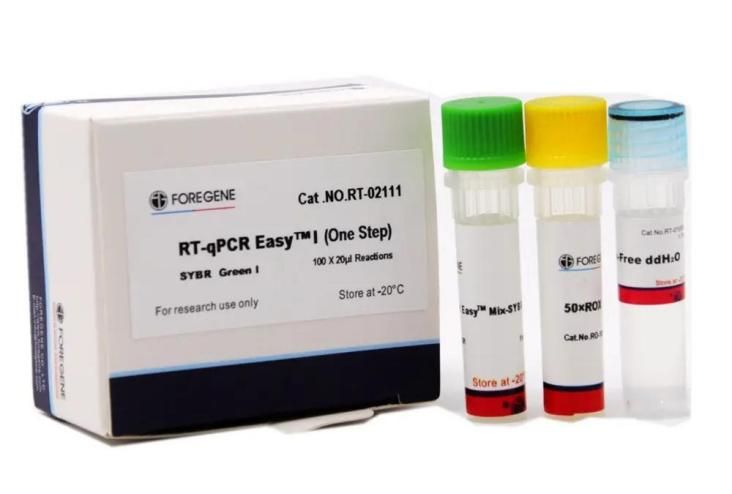
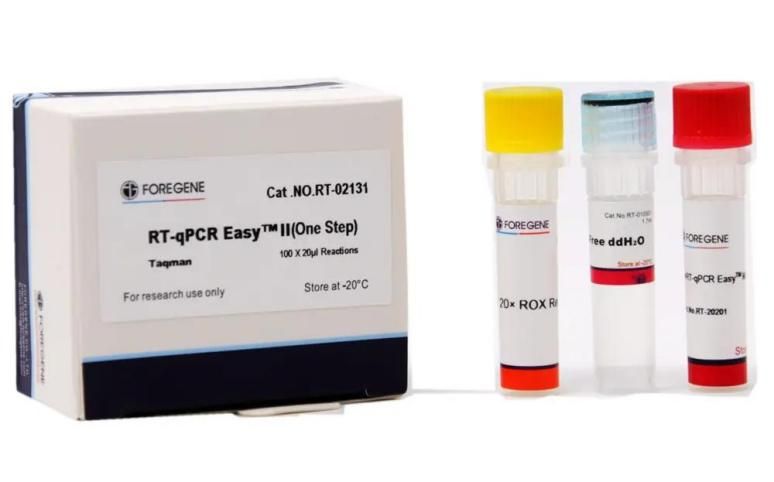
Пов’язаний комплект RT-qPCR
У наборі використовується унікальний реагент зворотної транскрипції Foregene та ДНК-полімераза Foregene HotStar Taq у поєднанні з унікальною реакційною системою для ефективного підвищення ефективності ампліфікації та специфічності реакції.
Час публікації: 23 квітня 2023 р