На ранній стадії спалаху, завдяки швидкому розвитку, швидка діагностика підозрюваних пацієнтів є ключем до запобігання COVID-19.Деякі схвалені реагенти для виявлення нуклеїнових кислот мають короткий час розробки, і виникають такі проблеми, як поспішне підтвердження продуктивності, недостатня оптимізація реагентів і великі відмінності між партіями;Проблеми різних клінічних лабораторій у різних аспектах процесу визначення нуклеїнових кислот також можуть вплинути на точність результатів визначення нуклеїнових кислот.У цій статті буде зосереджено увагу на ключових зв’язках і моментах поточного виявлення нуклеїнових кислот SARS-CoV-2, а також проаналізовано проблеми хибнонегативних і позитивних повторних досліджень виявлення нуклеїнових кислот у лабораторії та клінічну невідповідність.
Принципи виявлення нуклеїнової кислоти SARS-CoV-2
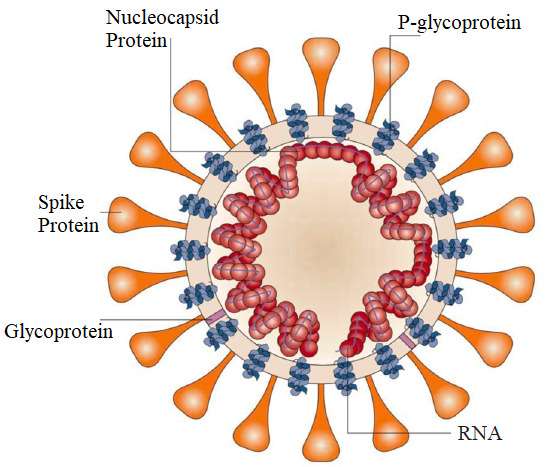
SARS-CoV-2 — це РНК-вірус із послідовністю геному близько 29 кб, з 10 генами, які можуть ефективно кодувати 10 білків.Віруси складаються з РНК і білка, а зовнішній шар – це зовнішнє покриття, що складається з ліпідів і глікопротеїнів.Всередині білковий капсид огортає РНК, захищаючи тим самим РНК, що легко розкладається (P1).
P1 Структура SARS-COV-2
Віруси вторгаються в клітини через специфічні рецептори клітинної поверхні, щоб викликати інфекцію, і використовують клітини-господарі для реплікації.
Принцип виявлення вірусної нуклеїнової кислоти полягає в експонуванні вірусної РНК через клітинний лізат, а потім для виявлення в режимі реального часу використовують флуоресцентну полімеразну ланцюгову реакцію зворотної транскрипції (RT-PCR).
Ключ до принципу виявлення полягає у використанні праймерів і зондів для досягнення «цільової відповідності» послідовностей нуклеїнових кислот, тобто для пошуку послідовності нуклеїнової кислоти SARS-CoV-2, яка відрізняється від інших вірусів приблизно на 30 000 основ (схожість нуклеїнової кислоти з іншими вірусами) «Низька» область), проектування праймерів і зондів.
Праймери та зонди добре збігаються зі специфічною ділянкою нуклеїнової кислоти SARS-CoV-2, тобто специфічність дуже висока.Якщо результат флуоресцентної RT-PCR ампліфікації в режимі реального часу зразка для тестування є позитивним, це доводить наявність SARS-CoV-2 у зразку.Див. P2.
P2 Етапи визначення нуклеїнової кислоти SARS-CoV-2 (флуоресцентна ПЛР у реальному часі)
Умови та вимоги лабораторії для виявлення нуклеїнової кислоти SARS-CoV-2
Лабораторії тестування нуклеїнових кислот є найбільш ідеальними для середовищ із негативним тиском, і вони повинні приділяти увагу моніторингу тиску, підтримувати потік повітря та видаляти аерозолі.Персонал, що займається тестуванням нуклеїнових кислот, повинен мати відповідну кваліфікацію, пройти відповідну підготовку з полімеразної ланцюгової реакції та пройти оцінювання.Лабораторія має суворо керуватися, бути зонованою, а сторонньому персоналу вхід суворо заборонений.Чисте приміщення слід провітрювати та дезінфікувати на місці.Відповідні предмети розміщуються по зонах, чисті та брудні відокремлюються, вчасно замінюються та дезактивуються на місці.Звичайна дезінфекція: для великих площ основним рішенням є дезінфікуючий засіб, що містить хлор, а для невеликих площ можна використовувати 75% спирт.Хорошим способом боротьби з аерозолями є відкривання вікон для провітрювання, а також знезараження повітря можна проводити за допомогою ультрафіолетових променів, фільтрації та знезараження повітря.
Ключові ланки та параметри визначення нуклеїнової кислоти SARS-CoV-2 (флуоресцентна ПЛР в реальному часі)
Хоча лабораторії зазвичай приділяють пильну увагу «виявленню» нуклеїнової кислоти, насправді «вилучення» нуклеїнової кислоти також є одним із ключових кроків для успішного виявлення, що тісно пов’язане зі збором і зберіганням зразків вірусу.
В даний час найбільш широко використовувані респіраторні зразки, такі як мазки з носоглотки, використовують другий метод, який є інактиваційним (консервуючим) розчином, приготовленим на основі екстракції нуклеїнової кислоти та розчину для лізису.З одного боку, цей розчин для збереження вірусу може денатурувати білок вірусу, втратити його активність і більше не бути інфекційним, а також підвищити безпеку етапу транспортування та виявлення;з іншого боку, він може безпосередньо зламати вірус, щоб вивільнити нуклеїнову кислоту, усунути фермент, що розкладає нуклеїнову кислоту, і запобігти вірусу.РНК деградує.
Розчин зразка вірусу, виготовлений на основі розчину лізису екстракції нуклеїнової кислоти.Основними компонентами є збалансовані солі, хелатурація етилендіамінеттраоцтової кислоти, гуанідин солі (гуанідин ізотіоціанат, гуанідин гідрохлорид тощо), аніонні поверхнево-активні речовини (додеекан) сульфат натрію), катічний поверхневий речовина (тетрадецил триметиновий оксалат), фенол, 8-гріолінолат, фенолл, 8-г-гріолінолат, фенолл, фенол, 8-г-гріолінолат, фенолл, 8-гріолінолат, фенолл, фенол, 8-гріолінолат, фенолл inase k та інші кілька або більше компонентів.В даний час існує багато типів наборів для екстракції нуклеїнових кислот, а також використовуються різні реагенти для екстракції та очищення нуклеїнових кислот.Навіть якщо використовується той самий реагент для екстракції та очищення нуклеїнової кислоти, процедури екстракції для кожного набору відрізняються.
Наразі продукти наборів для виявлення нуклеїнових кислот, схвалені Національним управлінням медичних продуктів, вибираються на основі генів ORF1ab, E та N у геномі SARS-CoV-2.Принципи виявлення різних продуктів в основному однакові, але їхні праймери та конструкції зондів відрізняються.Існують одноцільові сегменти (ORF1ab), подвійні цільові сегменти (ORF1ab, N або E) і трицільові сегменти (ORF1ab, N і E).Різницю між виявленням та інтерпретацією, екстракцією нуклеїнової кислоти та реакційною системою флуоресцентної RT-PCR у режимі реального часу слід див.Загальні ділянки, праймери та послідовності зондів, ампліфіковані за допомогою флуоресцентної RT-PCR у реальному часі, показані на P3.
P3 Розташування мішені амплікону SARS-CoV-2 у геномі та послідовності праймерів і зондів
Інтерпретація результатів визначення нуклеїнової кислоти SARS-CoV-2 (Rтак-Tім'я флуоресцентної RT-PCR)
«План профілактики пневмонії та контролю за інфекцією SARS-CoV-2 (друге видання)» вперше уточнив критерії для оцінки результатів ампліфікації одного гена:
1. Немає Ct або Ct≥40 є негативним;
2. Ct<37 позитивний;
3. Значення Ct 37-40 є областю сірого.Рекомендується повторити дослід.Якщо результат повторного виконання Ct<40 і крива ампліфікації має явні піки, зразок вважається позитивним, інакше він є негативним».
Третє видання довідника та четверте видання довідника продовжили вищевказані критерії.Однак через різні мішені, які використовуються в комерційних наборах, вищезазначене 3-е видання посібника не містить критеріїв для визначення комбінації мішеней, наголошуючи на тому, що перевагу мають інструкції, надані виробником.Починаючи з п’ятого видання настанов, було уточнено дві цілі, особливо критерії оцінки для однієї цілі, яку важко оцінити.Тобто, якщо лабораторія хоче підтвердити, що випадок позитивний на виявлення нуклеїнової кислоти SARS-CoV-2, має бути виконано 1 з 2 умов:
(1) Дві мішені SARS-CoV-2 (ORF1ab, N) в одному зразку виявляються позитивними за допомогою флуоресцентної RT-PCR у реальному часі.Якщо одна мішень є позитивною, необхідні повторний відбір зразків і повторне тестування.Якщо результати тесту є. Якщо єдина мішень все ще позитивна, вона вважається позитивною.
(2) Два зразки флуоресцентної RT-PCR у режимі реального часу показали одну позитивну мішень одночасно або два зразки одного типу показали одну мішень позитивний результат тесту, який можна оцінити як позитивний.Однак у рекомендаціях також наголошується, що негативні результати аналізу нуклеїнової кислоти не можуть виключити інфекцію SARS-CoV-2.Необхідно виключити фактори, які можуть спричинити хибнонегативні результати, включаючи низьку якість зразків (респіраторні зразки з ротоглотки та інших частин), надто ранній або надто пізній збір зразків, зразки не зберігалися, транспортувалися та оброблялися належним чином, і сама технологія мала проблеми (варіації вірусу, інгібування ПЛР) тощо.
Причини помилкових негативних результатів при виявленні SARS-CoV-2
Поняття «хибнонегативний» у тестуванні на нуклеїнову кислоту, яке зараз стосується, часто стосується «хибнонегативного результату», коли результати тесту на нуклеїнову кислоту не відповідають клінічним проявам, тобто клінічні симптоми та результати візуалізації викликають серйозну підозру на COVID-19, але тести на нуклеїнову кислоту завжди «негативні» багато разів.Клінічний лабораторний центр НСЗУ пояснив «хибнонегативний» тест на SARS-CoV-2.
(1) У клітинах інфікованої людини є певна кількість вірусу.Існуючі дані показують, що після зараження організму вірусом, вірус потрапляє в горло через ніс і рот, потім в трахею і бронхи, а потім досягає альвеол.Інфікована людина переживає інкубаційний період, легкі симптоми, а потім процес важких симптомів і різні стадії захворювання.І кількість вірусу в різних частинах тіла різна.
З точки зору вірусного навантаження типів клітин, альвеолярні епітеліальні клітини (нижні дихальні шляхи)> епітеліальні клітини дихальних шляхів (верхні дихальні шляхи)> фібробласти, ендотеліальні клітини та макрофаги тощо;з типу зразка, альвеолярний лаваж (найбільш відмінний)> мокрота при глибокому кашлі> мазок з носоглотки> мазок з ротоглотки> кров.Крім того, вірус також можна виявити в калі.Однак, враховуючи зручність операції та сприйняття пацієнтів, зазвичай використовується клінічний порядок зразків: мазок з ротоглотки> мазок з носоглотки> промивна рідина бронхів (складна операція) і глибоке мокротиння (зазвичай сухий кашель, важко отримати).
Тому кількість вірусу в клітинах ротоглотки або носоглотки деяких пацієнтів невелика або вкрай мала.Якщо взяти для дослідження тільки зразки ротоглотки або носоглотки, нуклеїнова кислота вірусу не буде виявлена.
(2) Під час збору зразків не було зібрано клітин, що містять вірус, або нуклеїнова кислота вірусу не була ефективно збережена.
[① Неправильне місце збору, наприклад, під час збору мазків з ротоглотки недостатня глибина збору, зібрані мазки з носоглотки не збираються глибоко в носовій порожнині тощо. Більшість зібраних клітин можуть бути клітинами, вільними від вірусів;
②Тампони для взяття проб використовуються неправильно.Наприклад, синтетичні волокна, такі як поліетиленове волокно, поліефірне волокно та поліпропіленове волокно, рекомендовані для виготовлення головки тампона.Натуральні волокна, такі як бавовна, використовуються в фактичній роботі (сильна адсорбція білка і їх нелегко вимити) і нейлонові волокна (погане водопоглинання, що призводить до недостатнього об’єму проби);
③Неправильне використання пробірок для зберігання вірусів, наприклад використання поліпропіленових або поліетиленових пластикових пробірок для зберігання, які легко поглинають нуклеїнові кислоти (ДНК/РНК), що призводить до зниження концентрації нуклеїнової кислоти в розчині для зберігання.На практиці для зберігання вірусних нуклеїнових кислот рекомендується використовувати поліетилен-пропіленовий полімерний пластик і деякі спеціально оброблені поліпропіленові пластикові контейнери.]
[① Неправильне місце збору, наприклад, під час збору мазків з ротоглотки недостатня глибина збору, зібрані мазки з носоглотки не збираються глибоко в носовій порожнині тощо. Більшість зібраних клітин можуть бути клітинами, вільними від вірусів;
②Тампони для взяття проб використовуються неправильно.Наприклад, синтетичні волокна, такі як поліетиленове волокно, поліефірне волокно та поліпропіленове волокно, рекомендовані для виготовлення головки тампона.Натуральні волокна, такі як бавовна, використовуються в фактичній роботі (сильна адсорбція білка і їх нелегко вимити) і нейлонові волокна (погане водопоглинання, що призводить до недостатнього об’єму проби);
③Неправильне використання пробірок для зберігання вірусів, наприклад використання поліпропіленових або поліетиленових пластикових пробірок для зберігання, які легко поглинають нуклеїнові кислоти (ДНК/РНК), що призводить до зниження концентрації нуклеїнової кислоти в розчині для зберігання.На практиці для зберігання вірусних нуклеїнових кислот рекомендується використовувати поліетилен-пропіленовий полімерний пластик і деякі спеціально оброблені поліпропіленові пластикові контейнери.]
(4) Робота клінічної лабораторії не стандартизована.Умови транспортування та зберігання зразків, стандартизована робота клінічних лабораторій, інтерпретація результатів і контроль якості є ключовими факторами для забезпечення точності та достовірності результатів аналізів.За результатами зовнішньої оцінки якості, проведеної ДУ «Клінічний лабораторний центр НСЗУ» 16-24 березня 2020 року, з 844 лабораторій, які отримали дійсні результати, 701 (83,1%) є кваліфікованими, а 143 (16,9%) – ні.Кваліфікований, загальні умови лабораторного тестування хороші, але різні лабораторії все ще мають відмінності в здатності персоналу працювати, здатності одноцільової інтерпретації позитивних зразків і контролю якості.
Як зменшити хибнонегативний результат виявлення нуклеїнової кислоти SARS-CoV-2?
Зменшення помилкових негативних результатів при виявленні нуклеїнових кислот слід оптимізувати за чотирма аспектами створення помилкових негативних результатів.
(1) У клітинах інфікованої людини є певна кількість вірусу.Концентрація вірусу в різних частинах тіла підозрюваних інфікованих людей буде різною в різний час.Якщо глотки немає, це може бути в промивній рідині бронхів або калі.Якщо кілька типів зразків можна зібрати одночасно або на різних стадіях прогресування захворювання для тестування, це допоможе уникнути хибно негативних результатів.
(2) Клітини, що містять вірус, слід зібрати під час збору зразків.Цю проблему можна значною мірою вирішити шляхом посилення підготовки збирачів проб.
(3) Надійні реагенти IVD.Проводячи дослідження щодо оцінки ефективності виявлення реагентів на національному рівні та обговорюючи існуючі проблеми, ефективність виявлення реагентів можна покращити, а чутливість аналізу можна покращити.
(4) Стандартизована робота клінічних лабораторій.Шляхом посилення підготовки персоналу лабораторії, постійного вдосконалення системи управління якістю лабораторії, забезпечення розумного розподілу та вдосконалення здатності персоналу виявляти, можна зменшити помилкові негативні результати через неправильні лабораторні операції.
Причини повторного позитивного результату тесту на нуклеїнову кислоту SARS-CoV-2 у одужали та виписаних пацієнтів
У «Плані діагностики та лікування COVID-19 (Пробне сьоме видання)» чітко зазначено, що одним із критеріїв виліковування та виписки пацієнтів із COVID-19 є те, що два послідовних зразки дихальних шляхів мають негативний тест на нуклеїнову кислоту (принаймні через 24 години), але дуже мало тестів на нуклеїнову кислоту SARS-CoV-2 знову виявився позитивним у виписаних пацієнтів з різних причин.
(1) SARS-CoV-2 — новий вірус.Необхідно додатково зрозуміти його патогенний механізм, повну картину викликаного захворювання та особливості перебігу захворювання.Тому, з одного боку, необхідно посилити ведення виписаних пацієнтів і проводити 14-денне медичне спостереження.Проводити подальше спостереження, моніторинг здоров'я та медичне керівництво для поглиблення розуміння всього процесу виникнення, розвитку та результату захворювання.
(2) Пацієнт може знову інфікуватися вірусом.Академік Чжун Наньшань сказав: оскільки у вилікуваних пацієнтів є антитіла, антитіла можуть знищити SARS-CoV-2, коли вони знову вторгнуться.Є багато причин, які можуть бути причиною одужання пацієнта, або це може бути пов'язано з мутацією вірусу, або навіть причиною лабораторного дослідження.Якщо це сам вірус, мутація SARS-CoV-2 може спричинити неефективність антитіл, вироблених одужалим пацієнтом, проти мутованого вірусу.Якщо пацієнт знову інфікується мутованим вірусом, тест на нуклеїнову кислоту може бути знову позитивним.
(3) Що стосується лабораторних методів тестування, кожен метод тестування має свої обмеження.Виявлення нуклеїнової кислоти SARS-CoV-2 обумовлено вибором послідовності гена, складом реагентів, чутливістю методу та іншими причинами, що призводить до того, що існуючі набори мають власні нижні межі виявлення.Після лікування пацієнта кількість вірусу в організмі зменшується.Коли вірусне навантаження в досліджуваному зразку буде нижче нижньої межі виявлення, з’явиться «негативний» результат.Однак цей результат не означає, що вірус в організмі повністю зник.Вірус може бути після припинення лікування.Відродження», продовжуйте копіювати.Тому рекомендується проводити огляд один раз на тиждень протягом 2-4 тижнів після виписки.
(4) Нуклеїнова кислота є генетичним матеріалом вірусу.Вірус гине після того, як пацієнт пройшов противірусне лікування, але залишилися фрагменти вірусної РНК залишаються в організмі людини і не виводяться з організму повністю.Іноді, за певних обставин, його можна зберегти.Тривалий час, і в цей час тест на нуклеїнові кислоти буде «минущим» позитивним.При збільшенні терміну відновлення пацієнта, після того, як залишкові фрагменти РНК в організмі поступово вичерпуються, результат тесту на нуклеїнову кислоту може стати негативним.
(5) Результат тесту на нуклеїнову кислоту SARS-CoV-2 лише підтверджує наявність або відсутність вірусної РНК і не може підтвердити активність вірусу та його трансмісивність.Необхідно довести, чи пацієнт, у якого знову позитивний тест на нуклеїнову кислоту, знову стане джерелом інфекції.Необхідно провести посів вірусу на клінічних зразках і культивувати «живий» вірус, щоб довести його інфекційність.
Резюме
Підводячи підсумок, неможливо повністю уникнути помилкових негативних результатів тесту на нуклеїнову кислоту SARS-CoV-2, позитивного результату повторного тесту та інших станів, які не відповідають клінічним проявам.Під час фактичного скринінгу та тестування рекомендується поєднувати клінічні симптоми, візуалізаційні дослідження (КТ) та результати лабораторних досліджень (тест на нуклеїнову кислоту + тест на вірус-специфічні антитіла) для комплексної діагностики, щоб запобігти пропуску діагнозу та неправильному діагнозу.Якщо результати тесту виявляються явно невідповідними клінічним проявам, рекомендується провести комплексний аналіз усієї ланки тестування (збір зразків, циркуляція та ланки обробки), щоб виключити раннє інфікування вірусом SARS-CoV-2, рецидиву інфікування чи поєднання з іншими респіраторними вірусними інфекціями тощо.Якщо умови дозволяють, рекомендується зібрати більш чутливі зразки, такі як мокротиння або альвеолярний лаваж, для повторного дослідження.
Супутні товари:
Час публікації: 03 вересня 2021 р