1. Базові знання (якщо ви хочете побачити експериментальну частину, будь ласка, перейдіть безпосередньо до другої частини)
Будучи похідною реакцією звичайної ПЛР, ПЛР у реальному часі головним чином відстежує зміну кількості продукту ампліфікації в кожному циклі реакції ампліфікації ПЛР у режимі реального часу через зміну сигналу флуоресценції та кількісно аналізує початковий шаблон через співвідношення між значенням ct та стандартною кривою.
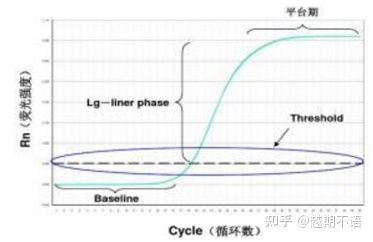
Специфічні дані RT-PCR такібазова лінія, поріг флуоресценціїіЗначення Ct.
| базова лінія: | Значення флуоресценції 3-го-15-го циклу є базовим (базовим), яке викликано випадковою похибкою вимірювання. |
| Поріг (поріг): | Відноситься до межі виявлення флуоресценції, встановленої у відповідній позиції в області експоненціального зростання кривої ампліфікації, як правило, у 10 разів більше стандартного відхилення базової лінії. |
| значення CT: | Це кількість циклів ПЛР, коли значення флуоресценції в кожній реакційній пробірці досягає порогового значення. Значення Ct обернено пропорційне кількості початкового шаблону. |
Загальні методи маркування для RT-PCR:
| метод | перевага | недолік | сфера застосування |
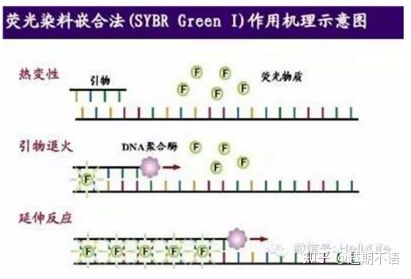
| SYBR GreenⅠ | Широке застосування, чутливий, дешевий і зручний | Вимоги до грунтовки високі, схильні до неспецифічних смуг | Він підходить для кількісного аналізу різних цільових генів, дослідження експресії генів і дослідження трансгенних рекомбінантних тварин і рослин. |
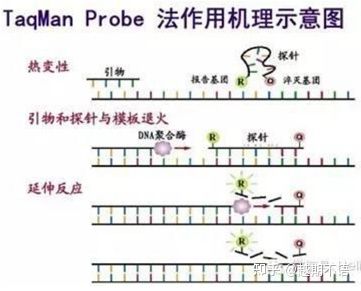
| TaqMan | Хороша специфічність і висока повторюваність | Ціна висока і підходить тільки для конкретних цілей. | Виявлення збудників, дослідження генів стійкості до ліків, оцінка ефективності препаратів, діагностика генетичних захворювань. |
| молекулярний маяк | Висока специфічність, флуоресценція, низький фон | Ціна висока, підходить тільки для конкретної мети, конструкція складна, ціна висока. | Специфічний генний аналіз, аналіз SNP |
2. Експериментальні етапи
2.1 Про експериментальне угруповання- у групі має бути кілька лунок і мають бути біологічні повтори.
| ① | Пустий контроль | Використовується для визначення стану росту клітин в експериментах |
| ② | Негативний контроль siRNA (неспецифічна послідовність siRNA) | Продемонструвати специфічність дії RNAi.siRNA може викликати неспецифічну відповідь на стрес у концентрації 200 нМ. |
| ③ | Контроль реагентів трансфекції | Виключити токсичність трансфекційного реагенту для клітин або вплив на експресію цільового гена |
| ④ | siRNA проти цільового гена | Збити експресію цільового гена |
| ⑤ (необов'язково) | позитивна siRNA | Використовується для усунення несправностей експериментальної системи та операційних проблем |
| ⑥ (необов'язково) | Флуоресцентна контрольна siRNA | Ефективність трансфекції клітин можна спостерігати за допомогою мікроскопа |
2.2 Принципи проектування грунтовки
| Збільшений розмір фрагмента | Бажано на 100-150 bp |
| Довжина грунтовки | 18-25 п.н |
| Вміст GC | 30%-70%, переважно 45%-55% |
| значення Tm | 58-60 ℃ |
| Послідовність | Уникайте безперервного T/C;A/G безперервний |
| 3 кінцева послідовність | Уникайте GC rich або AT rich;кінцева основа переважно G або C;найкраще уникати Т |
| Взаємодоповнюваність | Уникайте комплементарних послідовностей з більш ніж 3 основ у праймері або між двома праймерами |
| Специфіка | Використовуйте бласт-пошук, щоб підтвердити специфічність праймера |
①SiRNA видоспецифічна, і послідовності різних видів будуть різними.
②SiRNA упакована в ліофілізований порошок, який можна стабільно зберігати протягом 2-4 тижнів при кімнатній температурі.
2.3 Інструменти або реактиви, які необхідно підготувати заздалегідь
| Буквар (внутрішнє посилання) | Включаючи прямий і зворотний два |
| Праймери (цільовий ген) | Включаючи прямий і зворотний два |
| Цільова Si РНК (3 смужки) | Як правило, компанія синтезує 3 смужки, а потім вибирає одну з трьох за допомогою RT-PCR |
| Набір для трансфекції | Lipo2000 тощо. |
| Набір для швидкого виділення РНК | Для екстракції РНК після трансфекції |
| Набір для швидкої зворотної транскрипції | для синтезу кДНК |
| Набір для ПЛР-ампліфікації | 2×Super SYBR Green qPCR Master Mix |
2.4 Щодо питань, на які необхідно звернути увагу на конкретних етапах експерименту:
①процес трансфекції siRNA
1. Для посіву ви можете вибрати 24-лунковий планшет, 12-лунковий планшет або 6-лунковий планшет (середня концентрація РНК, запропонована в кожній лунці 24-лункового планшета, становить близько 100-300 нг/мкл), а оптимальна щільність трансфекції клітин становить приблизно 60%-80%.
2. Етапи трансфекції та особливі вимоги суворо відповідають інструкціям.
3. Після трансфекції зразки можна зібрати протягом 24-72 годин для виявлення мРНК (RT-PCR) або виявлення білка протягом 48-96 годин (WB)
② Процес екстракції РНК
1. Запобігайте забрудненню екзогенними ферментами.В основному це суворе носіння масок і рукавичок;використання стерилізованих наконечників піпеток і пробірок EP;вода, яка використовується в експерименті, не повинна містити РНКази.
2. Рекомендується робити двічі, ніж запропоновано в наборі для швидкого відсмоктування, що дійсно покращить чистоту та врожайність.
3. Відпрацьована рідина не повинна торкатися колонки РНК.
③ Кількісне визначення РНК
Після виділення РНК її можна кількісно визначити безпосередньо за допомогою Nanodrop, і мінімальне значення може становити лише 10 нг/мкл.
④Процес зворотної транскрипції
1. Через високу чутливість RT-qPCR для кожного зразка слід зробити принаймні 3 паралельні лунки, щоб запобігти занадто великій різниці наступного Ct або занадто великому SD для статистичного аналізу.
2. Не заморожуйте та не розморожуйте Master mix повторно.
3. Кожну трубку/отвір необхідно замінити новим наконечником!Не використовуйте постійно один і той самий наконечник піпетки для додавання зразків!
4. Плівку, прикріплену до 96-лункового планшета після додавання зразка, необхідно розгладити планшетом.Найкраще відцентрифугувати перед тим, як поставити його в машину, щоб рідина зі стінки трубки могла стікати вниз і видаляти бульбашки повітря.
⑤Аналіз загальної кривої
| Відсутність періоду логарифмічного зростання | Можливо висока концентрація шаблону |
| Немає значення КТ | Неправильні кроки для виявлення флуоресцентних сигналів; деградація праймерів або зондів – її цілісність можна виявити електрофорезом у ПААГ; недостатня кількість шаблону; деградація шаблонів – уникнення введення домішок і повторного заморожування та розморожування при підготовці зразка; |
| Ct>38 | Низька ефективність посилення;продукт ПЛР занадто довгий;різні компоненти реакції деградують |
| Лінійна крива підсилення | Зонди можуть частково руйнуватися через повторювані цикли заморожування-відтавання або тривалий вплив світла |
| Особливо велика різниця в дублюючих отворах | Реакційний розчин не повністю розплавлений або реакційний розчин не змішаний;Термічна ванна приладу ПЛР забруднена флуоресцентними речовинами |
2.5 Про аналіз даних
Аналіз даних КПЦР можна розділити на відносну та абсолютну кількісну оцінку.Наприклад, клітини в групі лікування порівняно з клітинами в контрольній групі,
Скільки разів змінюється мРНК гена Х, це відносна кількісна оцінка;у певній кількості клітин — мРНК гена X
Скільки є копій, це абсолютна кількість.Зазвичай у лабораторії ми найчастіше використовуємо відносний кількісний метод.Зазвичай,метод 2-ΔΔctвикористовується найчастіше в експериментах, тому тут буде детально представлено лише цей метод.
Метод 2-ΔΔct: Отриманий результат є різницею в експресії цільового гена в експериментальній групі відносно цільового гена в контрольній групі.Необхідно, щоб ефективність ампліфікації як цільового гена, так і внутрішнього еталонного гена була близькою до 100%, а відносне відхилення не повинно перевищувати 5%.
Метод розрахунку такий:
Δct контрольна група = значення ct цільового гена в контрольній групі – значення ct внутрішнього еталонного гена в контрольній групі
Δct експериментальна група = ct значення цільового гена в експериментальній групі – ct значення внутрішнього еталонного гена в експериментальній групі
ΔΔct=Δct експериментальна група-Δct контрольна група
Нарешті, обчисліть множник різниці в рівні експресії:
Change Fold=2-ΔΔct (відповідає функції excel POWER)
Супутні товари:
Час публікації: 20 травня 2023 р